فهرست مطالب

شرایط تأسیس و بهرهبرداری مراکز سل تراپی
تأسیس و بهرهبرداری بخش منوط به اخذ موافقت اصولی افزایش بخش از کمیسیون قانونی وزارت و درج در پروانه بهرهبرداری بیمارستان است. موافقت اصولی افزایش بخش به بیمارستانهای متقاضی تأسیس بخش پزشکی بازساختی و سلول درمانی که صلاحیت آنان به تأیید کمیسیون قانونی وزارت رسیده باشد، داده میشود. صدور موافقت اصولی، مجوزی برای شروع فعالیت بخش نبوده و بههیچعنوان قابلواگذاری به غیر نمیباشد. درصورت واگذاری موافقت اصولی یادشده به هر شکل به غیر، مجوز از درجه اعتبار ساقط بوده و اثری بر آن مترتب نخواهد بود. بر این اساس بازسازی و شروع هرگونه عملیات ساختمانی قبل از اخذ موافقت اصولی و تأیید مکان و نقشهها توسط کارشناسان دانشگاه، ممنوع بوده و مسئولیت هرگونه ضرر و زیان به عهده متقاضی خواهد بود. متقاضی مکلف است مراحل اجرای موافقت اصولی و مفاد قرارداد، مبنی بر پیشرفت کار را به همراه مستندات لازم حداقل هر ۶ ماه یکبار به معاونت دانشگاه/ دانشکده متبوع اطلاع دهد. در صورت عدم ارائه گزارش یا عدم اجرای تعهدات مصرح در قرارداد در موعد مقرر، معاونت دانشگاه/ دانشکده مکلف است نسبت به ارجاع موضوع به کمیسیون قانونی وزارت جهت تعیین تکلیف اقدام و ضمن ابلاغ مراتب به مؤسس رونوشت آن را به معاونت ارسال نماید.
در حال حاضر مدت اعتبار و تمدید موافقت اصولی صادره بر اساس مفاد قرارداد منعقده بین معاونت و متقاضی بوده و در صورت عدم امکان تکمیل مدارک در مدت قرارداد تأسیس، تمدید آن منوط به ارائه گزارش و مستندات پیشرفت کار مورد تأیید معاونت و تأیید نهائی کمیسیون قانونی وزارت خواهد بود.
به استناد آییننامه اجرایی ماده ۸ قانون تشکیل وزارت بهداشت، درمان و آموزش پزشکی، رعایت مفاد و شرایط قرارداد در هر یک از موافقتهای اصولی براساس جدول زمانی مقرر و منطبق با هر یک از بندهای آن الزامی میباشد. در صورت عدم اجرای بند قرارداد در موعد مقرر، موافقت اصولی بدون نیاز به تصمیم کمیسیون قانونی وزارت، از درجه اعتبار ساقط میگردد.
بهرهبرداری و فعالیت بخش سل تراپی
در حال حاضر و بر اساس آخرین دستورالعمل ابلاغی وزارت بهداشت، بهره برداری و فعالیت بخش سل تراپی منوط به انجام اقدامات ذیل میباشد:
- ثبت و ارسال درخواست و مدارک موردنیاز از طریق سامانه الکترونیکی صدور پروانههای وزارت براساس ضوابط و مقررات جهت افزایش بخش و اخذ موافقت اصولی
- ارائه و تأیید مدارک جهت اخذ پروانه بهرهبرداری و مسئول فنی طبق ضوابط و زمانبندی ابلاغی در موافقت اصولی. این مدارک شامل موارد زیر می باشند :
- مدرک دانشنامه تخصصی پزشکی از دانشگاهها/ دانشکدههای علوم پزشکی وزارت بهداشت، درمان و آموزش پزشکی در یکی از خدمات درمانی ارائهشده در بخش جهت صدور پروانه مسئول فنی
- پروانه اشتغال (مطب) در شهر موردتقاضا جهت صدور پروانه مسئول فنی
- گواهینامه دوره مسئول فنی بخش پزشکی بازساختی و سلول درمانی
- گواهی عدم سوءپیشینه کیفری جهت صدور پروانه مسئول فنی
- گواهی عدم محکومیت انتظامی از سازمان نظام پزشکی جهت صدور پروانه مسئول فنی
- ارائه نقشه ساختمانی مورد تائید دفتر فنی دانشگاه/ دانشکده
- تأمین تجهیزات موردنیاز بخش
- صدور پروانه مسئول فنی بخش
- درج بخش در پروانه بهرهبرداری بیمارستان و صدور پروانه مسئول فنی
- آغاز فعالیت و اعلام شروع به کار بخش به دانشگاه/ دانشکده پس از صدور پروانه بهرهبرداری
زمان فعالیت بخش های سلول درمانی میتواند در نوبتهای کاری صبح/ عصر/ صبح و عصر/ شبانهروزی بوده و منوط به حضور مسئول فنی بخش میباشد. نوع خدمات قابل ارائه توسط بخش، منوط به وجود بخشهای بستری تخصصی مربوطه در پروانه بهرهبرداری بیمارستان میباشد. این مورد شامل یک استثنا می باشد. ارائه خدمات پزشکی بازساختی و سلول درمانی که بهصورت کارآزمایی بالینی است بهشرط رعایت ضوابط انجام کارآزماییهای بالینی از شمول این موضوع خارج میباشد.
قابل توجه می باشد که صدور پروانه بهرهبرداری علاوه بر ترتیبات فوق، منوط به اخذ و ارائه تأییدیههای موردنیاز از سوی مراجع ذیصلاح و ذیربط قانونی ازجمله سازمان آتشنشانی، شهرداری، سازمان نظاممهندسی، وزارت کار و امور اجتماعی و سازمان ملی استاندارد ایران میباشد.
برای اطلاعات بیشتر در زمینه راه اندازی بخش سل تراپی با ما در تماس باشید. برای مطالعه بیشتر می توانید مقالات ذیل را مطالعه فرمایید:
- ضوابط تاسیس و راه اندازی مراکز سل تراپی- بخش دوم: وظایف مؤسس و مسئولین فنی در مراکز سلول درمانی، ضوابط پرسنل مراکز سلول درمانی
- ضوابط تاسیس و راه اندازی مراکز سل تراپی- بخش سوم: مدیریت کیفیت در مراکز سلول درمانی
- ضوابط تاسیس و راه اندازی مراکز سل تراپی- بخش چهارم: ضوابط ساختمانی، تجهیزاتی، ایمنی و بهداشتی مراکز سل تراپی
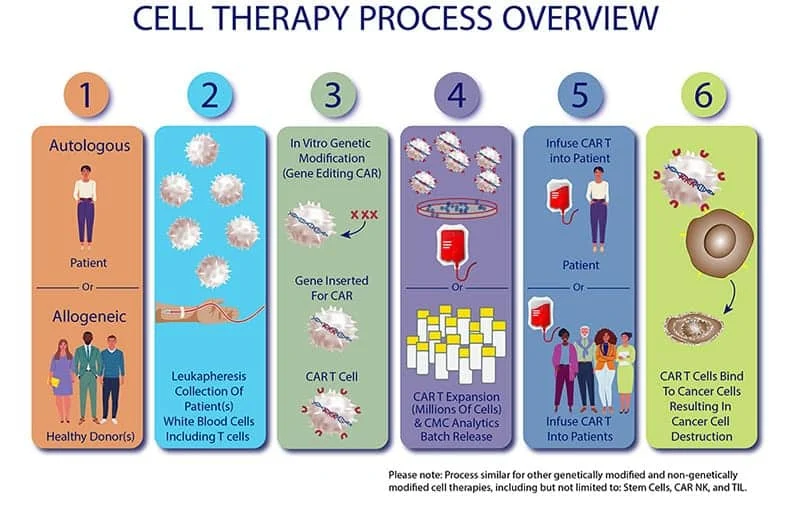
وظایف مؤسس و مسئولین فنی در مراکز سلول درمانی( سل تراپی)
یکی از مهمترین موارد راه اندازی مراکز سل تراپی حضور مسئول فنی مرتبط و نیز موسس می باشد. بر اساس آخرین ابلاغیه وزارت بهداشت ، درمان و آموزش پزشکی در خصوص مراکز ارائه دهنده خدمات سلول درمانی، هیئت موسس و مسئولین فنی شرح وظایفی متعددی را عهده دار می باشند. در ادامه به مهمترین این موارد اشاره خواهیم نمود.
“وظایف مؤسس” بخش سل تراپی
- معرفی مسئولین فنی بخش
- در صورت استعفاء یا پایان مدت قرارداد مسئول فنی بخش، مؤسس موظف است جایگزین وی را با معرفی فرد واجد شرایط درخواست نماید و رعایت کلیه شرایط احراز مسئول فنی در این خصوص الزامی است. درخواست مذکور میبایست حداقل سه ماه پیش از انقضای مدت قرارداد یا خاتمه کار صورت گیرد بهنحویکه بخش در هیچ زمانی بدون مسئول فنی نباشد.
- رعایت کلیه ضوابط، مقررات، دستورالعملها و تعرفههای مصوب مراجع ذیصلاح و ذیربط قانونی
- اجرای نظرات و پیشنهادات مسئول فنی بخش جهت اجرای امور پزشکی و فنی بر اساس ضوابط مربوط به بخش و فعالیت در چهارچوب سیاستهای تعیینشده وزارت متبوع
- برنامهریزی و سازماندهی مناسب بخش جهت ارائه خدمات مطلوب و جلب رضایت بیماران و رعایت منشور حقوق بیماران و پرسنل و رعایت موازین تأمین حفاظت فنی و ایمنی بیماران
- نظارت بر حسن اجرای استانداردهای مربوطه
- رفع نواقص و ایرادهای بخش در مدتی که توسط کارشناسان وزارت و یا معاونت یا مسئول فنی مربوطه اعلام میگردد.
- پاسخگویی به محاکم قضایی، معاونت درمان وزارت دانشگاه/ دانشکده و سایر مراجع ذیصلاح قضایی
- تهیه وسایل و امکانات لازم برای تأمین حفاظت فنی، ایمنی و سلامت کارکنان و ارائه آموزشهای لازم به کارکنان و نظارت بر ایمنی محیط کار مؤسسه، پرسنل و بیماران و رعایت ضوابط و استانداردهای ایمنی، حفاظت، آتشنشانی و رفع و همچنین اخذ گواهیهای لازم در زمینه ضوابط استانداردهای ایمنی بر محیط کار بخش، پرسنل و نواقص به وجود آمده بیماران از ارگانهای مرتبط
- کسب اطلاع از قوانین و مقررات و ضوابط و دستورالعملهای مربوطه و دسترسی به آنها
- تأمین تجهیزات و ملزومات پزشکی، مصرفی، دارویی و کلیه اقلام موردنیاز
- اجرا و رعایت الزامات قانونی مرتبط با ضوابط اعتباربخشی بخش
- مؤسس موظف است تمام ساختمان و تأسیسات و… که متعلق به او یا در اختیار اوست به هزینه خود بیمه کند و درصورت وقوع حادثه، جبران خسارتهای واردشده به عهده او است.
شرایط و شرح وظایف مسئول فنی
شرایط مسئول فنی بخش سلول درمانی به شرح زیر میباشد:
- پزشک متخصص دارای مدرک تخصصی پزشکی از دانشگاهها/ دانشکدهها یا مراکز مورد تأیید وزارت بهداشت، درمان و آموزش پزشکی مرتبط با یکی از خدمات درمانی ارائهشده در بخش
- دارا بودن پروانه اشتغال (مطب) در شهر موردتقاضا
- دارا بودن گواهینامه دوره مسئول فنی بخش پزشکی بازساختی و سلول درمانی
- احراز صلاحیتهای عمومی ازجمله ارائه گواهی عدم سوءپیشینه کیفری و عدم محکومیت انتظامی از سازمان نظام پزشکی
شرح وظایف مسئول فنی
- حضور مستمر و فعال در نوبتهای کاری بخش جهت انجام وظایف و مسئولیتهای امور فنی بخش طبق شرایط مندرج در پروانه مسئول فنی
- کسب اطلاع از قوانین و مقررات و ضوابط و دستورالعملهای وزارت بهداشت
- نظارت برحسن اجرای قوانین، مقررات، بخشنامهها، دستورالعملها، موازین علمی، استانداردها و پروتکلهای درمانی مرتبط با فعالیتهای ابلاغی بخش
- نظارت بر نحوه ارائه خدمت توسط پزشکان و کارکنان بخش و ابلاغ تذکرات لازم به آنان در جهت اجرای وظایف مربوطه و ارتقاء سطح کیفی خدمات درمانی
- نظارت بر حفظ شئون پزشکی و اخلاق حرفهای و همچنین اجرای ضوابط طرح انطباق امور فنی و اداری مؤسسات پزشکی با موازین شرع مقدس و منشور حقوق بیماران
- رسیدگی به شکایت بیماران در امور پزشکی و پاسخگویی به مراجع ذیربط
- نظارت بر تهیه، تنظیم و نگهداری پروندههای پزشکی بیماران
- نظارت بر جمعآوری اطلاعات و آمار مربوط به ارائه خدمات بخش و تهیه گزارشهای درخواستی وزارت/ دانشگاه/ دانشکده و سایر مراجع قانونی ذیربط با رعایت اصول محرمانگی
- نظارت بر دریافت تعرفههای مصوب قانونی و گزارش مکتوب آن به مؤسس جهت پیگیری و اصلاح آنها
- اعمال نظارت لازم برای جلوگیری از پرداختهای غیرمتعارف و خارج از صندوق پذیرش بیماران تحت پوشش بیمههای درمانی و جلوگیری از تحمیل هزینه و خدمات غیرضروری و نیز غیرمجاز به بیماران
- ثبت گزارش اقدامات انجامشده و رخدادهای مهم نوبتهای کاری در دفتر مخصوص، با امضاء و مهر مسئول فنی و نیز گزارش مشخصات و آمار بیماران فوتشده به معاونت دانشگاه/ دانشکده
- نظارت بر وضعیت بهداشتی، درمانی تجهیزات و ملزومات پزشکی و دارویی
- تشکیل جلسات منظم جهت هماهنگی با اعضای تیم پزشکی بازساختی و سلول درمانی بخش و تنظیم صورتجلسات مربوطه
- شرکت در جلسات هماهنگی مقرر از سوی دانشگاه/ دانشکده
- اجرا و رعایت الزامات قانونی ضوابط اعتباربخشی ابلاغی از سوی وزارت
- پاسخگویی به دانشگاه/ دانشکده/ معاونت
- پاسخگویی به مراجع قضایی ذیصلاح
- تهیه و تنظیم برنامه کاری قسمتهای مختلف بخش
- اجرای صحیح برنامه مدیریت کیفیت و ارزیابی سالانه نتایج آن

در حال حاضر مسئول فنی علاوه بر رعایت موارد فوق الذکر می بایست مقررات مربوط به حضور مسئول فن در بخش سل تراپی را نیز رعایت نماید. حضور مستمر مسئول فنی در بخش الزامی است. درصورتیکه مسئول فنی نتواند به دلایل موجه در بخش حاضر شود، مسئول فنی نوبت کاری دیگر میتواند حداکثر به مدت ۳ ماه بهعنوان جانشین موقت، وظایف وی را به عهده گیرد. درصورتیکه غیبت مسئول فنی بیش از ۳ ماه باشد، مؤسس موظف است جانشین واجد شرایط مسئول فنی را به معاونت دانشگاه/ دانشکده معرفی نماید.
مسئول فنی نمیتواند در نوبت کاری تعیینشده بخش، تحت هر عنوانی در محل کار دیگری فعالیت نماید. درصورتیکه مسئول فنی تمایل به ادامه کار نداشته باشد باید ۳ ماه قبل مراتب را بطور کتبی به مؤسس اعلام و همچنین در سامانه صدور پروانهها نسبت به ثبت انصراف خود اقدام نماید. در ظرف این مدت مؤسس موظف است نسبت به معرفی مسئول فنی جایگزین اقدام نموده پس از تصویب و تائید صلاحیت توسط کمیسیون قانونی وزارت، پروانه مسئول فنی جدید صادر گردد. در فاصله زمانی ثبت انصراف از ادامه فعالیت، کلیه مسئولیتهای مربوطه بر عهده مسئول فنی مستعفی میباشد.
در صورت ترک بخش توسط مسئول فنی و عدم انجام وظایف مندرج در این آییننامه بدون هماهنگی و رعایت مقررات مربوطه، کلیه مسئولیتهای قانونی تا زمان تعیین تکلیف ایشان بر عهده مسئول فنی خاطی بوده و مؤسس میبایست ضمن اقدام برابر ضوابط و مقررات، مراتب را به معاونت دانشگاه/ دانشکده جهت رسیدگی به مراجع ذیصلاح اطلاع دهد.
قبل از پایان مدت اعتبار پروانه مسئول فنی، مؤسس باید نسبت به تمدید اعتبار پروانه همان مسئول فنی و یا معرفی مسئول فنی جدید اقدام نماید و در غیر اینصورت ادامه فعالیت بخش ممنوع میباشد.
ضوابط پرسنلی بخش سلول درمانی
حداقل تعداد پرسنل موردنیاز بخش براساس نوع، حجم کار و تعداد وظایف محوله به کارکنان به شرح ذیل میباشد:
- یک نفر پزشک متخصص بهعنوان مسئول فنی بخش برای هر نوبت کاری
- حداقل یک پزشک متخصص درمانگر مرتبط با خدمات بخش و دارای حداقل ۲ سال تجربه در ارائه خدمات پزشکی بازساختی و سلول درمانی
تبصره: مسئول فنی میتواند پزشک متخصص درمانگر نیز باشد.
- یک کارشناس پرستاری در ارائه خدمات موردنیاز بخش جهت هر نوبت کاری
- یک کارشناس هوشبری باتجربه در زمینه احیای قلبی ریوی
در صورت اخذ مجوز انجام خدمات حداقل دست ورزی سلول، بافت و محصولات بر پایه سلول انسانی در بخش از معاونت، مؤسس موظف است برای این خدمت، فرد/ افراد صاحب صلاحیت را مطابق ضوابط مندرج در دستورالعمل حداقل دست ورزی که پس از تصویب این آیین نامه ظرف مدت ۲ ماه توسط معاونت تدوین و ابلاغ خواهد گردید بهکارگیری نماید.
وجود یک نفر پرسنل اداری جهت پذیرش و بایگانی مدارک پزشکی در هر نوبت کاری و نیز حداقل یک نفر نیروی خدماتی در حال حاضر الزامی می باشد.
مدیریت کیفیت در مراکز سلول درمانی
اجرای سیستم مدیریت کیفیت شامل برنامهای بهمنظور بهینهسازی کیفیت خدمات ارائهشده در بخش سل تراپی ( اعم از کارتی سل، مزانشیم و … ) میباشد و شامل مدیریت فعالیتهای مربوط به ارزیابی کیفیت، تضمین کیفیت و کنترل کیفیت میباشد.این برنامه بایستی بهصورت مکتوب و شامل چارت سازمانی افراد ارائهدهنده خدمت باشد و نحوه پاسخگویی و ارتباط بین افراد مسئول در کل فعالیتهای بخش که برای تضمین کیفیت خدمات بالینی حیاتی هستند را مشخص نماید. یک کتابچه راهنمای مدیریت کیفیت بخش برای سل تراپی (طرح مدیریت کیفیت[۱]) باید ایجاد شده و در بخش موجود باشد. به همین ترتیب پروتکلهای بالینی بهصورت چاپی یا نسخه الکترونیکی و نگهداری آنها در بخش جهت استفاده کارکنان بایستی تهیه گردد.
برنامه مدیریت کیفیت شامل اعتبار سنجی[۲] (مستندی که نشان میدهد عملکرد یک فرآیند خاص با الزامات برنامه بالینی مطابقت دارد. در برخی از مقالات به آن معتبر سازی و یا صحه گذاری نیز می گویند) و کیفیتسنجی[۳] (مستنداتی که نشان میدهد تجهیزات/ امکانات/ ابزارهای در حال استفاده توسط کاربر، مشخصات موردنیاز را دارا بوده بهدرستی کار میکند. در برخی مقالات به آن احراز کیفیت نیز می گویند) میباشد.
برای مطالعه بیشتر در باره اعتبارسنجی(معتبر سازی) و کیفیت سنجی(احراز کیفیت) می توانید به مقالات زیر مراجعه نمایید:
تفاوت بین احراز کیفیت صلاحیت و معتبرسازی
گزارش سیستم مدیریت کیفیت توسط مسئول فنی به شکل ادواری و به صورت فصلی به معاونت دانشگاه/ دانشکده متبوع می بایست ارائه میگردد.
چنانچه پژوهشی در بخش انجام میشود باید مدارک مربوط به آن شامل فرم رضایتنامه آگاهانه بیمار، پروپوزال طرح، تأییدیه کمیته اخلاق و فرمهای مربوط به مطالعه در بخش موجود باشد.
سیستم مدیریت کیفیت طراحی شده بایستی بر اساس استانداردهای بین المللی تدوین شود و شامل حداقل سرفصل های زیر باشد:
- پرسنل و نیروهای سازمان
- تضمین کیفیت
- آموزش
- انبارش
- پذیرش بیماران
- فرآیند ارائه خدمات
- ترخیص
- تامین مواد اولیه و کالاهای مورد نیاز بخش سل تراپی
- طراحی خدمات قابل ارائه
- معتبر سازی(صحه گذاری) و احراز کیفیت
- تجهیزات مورد استفاده
- کالیبراسیون تجهیزات
- زیر ساخت ها نظیر اتاق های تمیز(کلین روم) ، تاسیسات سرمایش و گرمایش بر طبق استانداردهای بین المللی بهمراه کلیه مستندات مربوطه در فاز های چهارگانه
- کنترل کیفیت در بخش های مختلف فرآیندها
- سیستم های نرم افزاری و کنترلی
- ردیابی در کلیه فرآیندهای جاری شده در سازمان
- ممیزی و ارزیابی های ادواری
مدیریت اطلاعات
بخش برای پذیرش هر بیمار ملزم به تشکیل پرونده پزشکی الکترونیکی میباشد. اطلاعات مربوط به پیگیری نتایج درمان برای هر بیمار میبایست طبق دستورالعملهای ابلاغی معاونت با نظارت مسئول فنی یا پزشک درمانگر جمعآوری و در پرونده الکترونیکی بیمار ثبت گردد.
کلیه مستندات شامل سوابق برنامه بالینی مربوط به مدیریت کیفیت، آموزش پرسنل، مدارک نگهداری تجهیزات، شکایتها و سایر موارد میبایست حداقل به مدت ۱۰ سال در بخش نگهداری شوند. نگهداری و بایگانی مدارک و پروندههای پزشکی بهصورت دستی یا رایانهای در بخش، تابع ضوابط و مقررات حفظ و نگهداری اسناد سازمان اسناد و کتابخانه جمهوری اسلامی ایران میباشد و امحای پروندههای پزشکی قدیمی نیز مستلزم اخذ مجوز از معاونت دانشگاه/ دانشکده مربوطه است.
برای اطلاعات بیشتر در زمینه طراحی سیستم مدیریت کیفیت و استقرار سیستم اطلاعات بیماران برای سل تراپی با ما در تماس باشید.
ضوابط ساختمانی، تجهیزاتی، ایمنی و بهداشتی مراکز سل تراپی
برای راه اندازی یک مرکز سلول درمانی توجه به ضوابط ساختمانی و تجهیزاتی مهمترین عامل می باشد. در بازرسی های صورت گرفته و ارزیابی کارشناسان ، وجود فضای فیزیکی مناسب بسیار مهم می نماید؛ از جمله مهمترین این موارد به داشتن اتاق های تمیز یا اصطلاحاً کلین روم(Clean Room) می توان اشاره کرد. وجود اتاق های تمیز با کلاس های مختلف، داشتن جریانهای مناسب از تردد پرسنل، مواد اولیه و تجهیزات مصرفی بسیار حائز اهمیت است. علاوه بر موارد فوق الذکر می بایست به فضا های تاثیر گذار بر فرایند سلول درمانی اشاره نمود.
فضاهای الزامی موردنیاز بخش سل تراپی
- اتاق مسئول فنی
- اتاق مشاوره و معاینه
- ایستگاه پرستاری
- اتاق عمل سرپایی جهت نمونهگیری، تزریق و یا پیوند سلول
- انبار دارو و تجهیزات
- اتاق پذیرش و مستندسازی
- در صورت اخذ مجوز انجام خدمات حداقل دست ورزی[۱] سلول، بافت و محصولات بر پایه سلول انسانی، فضای فیزیکی و تجهیزات لازم تابع دستورالعمل حداقل دست ورزی سلول بافت و محصولات خواهد بود. برای اطلاع در خصوص این دستورالعمل با ما در تماس باشید.
تزریق یا پیوند هر نوع فرآورده سلولی و پزشکی بازساختی میبایست در فضای مناسب و مطابق با دستورالعملهای درمانی معاونت انجام شود. در صورت نیاز به مراقبت از بیمار پس از تزریق سلول و یا نمونهگیری، متناسب با نوع بیماری و نوع مراقبتهای موردنیاز، بیمار به تشخیص و دستور پزشک درمانگر به بخش بستری مربوطه منتقل میگردد. فضای تولید فرآوردههای موضوع سل تراپی محدود به بیمارستان یا فضاهای تولید خارج بیمارستانی نبوده، مسئولیت بررسی و تائید فضای مذکور، شرایط تولید، ایجاد مستندات بر اساس الزامات، کنترل کیفیت، تضمین کیفیت و صدور پروانه ساخت آنها بر عهده سازمان غذا و دارو و طبق ضوابط و مقررات ابلاغی سازمان غذا و دارو میباشد. لازم به ذکر است که فرآوردههای با حداقل دست ورزی از قاعده فوق تبعیت نکرده، تابع دستورالعمل حداقل دست ورزی سلول، بافت و محصولات بر پایه سلول انسانی میباشد.
هرگونه تغییرات در فضای فیزیکی بخش مستلزم اخذ مجوز تأیید معاونت دانشگاه/ دانشکده مربوطه و مطابق با ضوابط و استانداردهای مصوب وزارت باشد. تائید نقشههای بخش سلول درمانی، توسط دفاتر مدیریت منابع فیزیکی دانشگاه/ دانشکده متبوع صرفاً بهمنظور رعایت استانداردهای تخصصی فضای فیزیکی مربوط به ارائه خدمات درمانی و بهداشتی بوده و نافی مسئولیت مؤسس بر اخذ تأییدیههای فنی و ایمنی و کلیه ضوابط عمومی ساختمان مربوطه در کلیه نقشههای ساختمانی اعم از معماری، آسانسور، سازه، برق و مکانیک، پیشبینی در امر حفاظت فنی و ایمنی و مانند آن از دستگاههای ذیربط ازجمله شهرداری، سازمان نظاممهندسی، سازمان آتشنشانی، سازمان ملی استاندارد و یا دستگاه اجرایی مربوطه نمیباشد.
برای استقرار شرایط مناسب در خصوص تاسیسات، باید کلیه موارد تاثیر گذار بر فرآیند درمان ، دارای اسناد معتبر سازی(Validation) و احراز کیفیت (Qualification) باشند. از جمله مواردیکه اسناد آن می بایست در بخش تضمین کیفیت و یا بخش اسناد مرکز قرار گیرد می توان به موارد زیر اشاره نمود:
- معتبرسازی و احراز کیفیت اتاق های تمیز
- معتبرسازی و احراز کیفیت سیستم هوای فشرده و HVAC
- معتبرسازی و احراز کیفیت آبساز ها
- معتبرسازی پاکسازی (Cleaning Validation)
- معتبرسازی و احراز کیفیت تجهیزات تاثیر گذار بر فرآیند درمان
وجود یک نقشه جامع معتبرسازی(Validatoin Master Plan) برای بخش درمانی توصیه می گردد. برای این منظور می توانید به مقاله زیر مراجعه نمایید:
برای مطالعه بیشتر در زمینه احراز کیفیت و معتبر سازی در حوزه سلول درمانی می توانید به مقالات زیر مراجعه نمایید:
برای اطلاعات بیشتر هم اکنون می توانید با کارشناسان توسعه کیفیت تماس حاصل نمایید