[et_pb_section fb_built=”1″ admin_label=”section” _builder_version=”4.4.2″ global_colors_info=”{}”][et_pb_row admin_label=”row” _builder_version=”3.25″ background_size=”initial” background_position=”top_left” background_repeat=”repeat” global_colors_info=”{}”][et_pb_column type=”4_4″ _builder_version=”3.25″ custom_padding=”|||” global_colors_info=”{}” custom_padding__hover=”|||”][et_pb_text admin_label=”Text” _builder_version=”4.4.2″ text_font=”b nazanin||||||||” header_font=”b nazanin||||||||” background_size=”initial” background_position=”top_left” background_repeat=”repeat” global_colors_info=”{}”]
سازمان غذا و دارو ایالات متحده امریکا
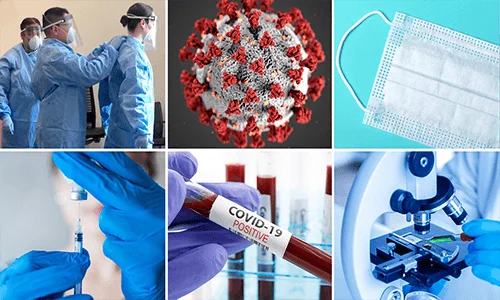
واکنش به بیماری کووید 19: تولیدکنندکان باید چه چیزهایی را درمورد صدورمجوز استفاده اورژانسی ازتجهیزات پزشکی و تجهیزات تشخیصی ازمایشگاهی (IVD ) تایید شده توسط سازمان غذا ودارو ایالات متحده آمریکا بدانند؟
ازآنجا که فراهمآورندگان مراقبت بهداشتی ایالات متحده آمریکا با کمبود تجهیزات وتجهیزات پزشکی حین شیوع بیماری همهگیرکووید 19 مواجه هستند، سازمان غذا ودارو به دنبال تسریع صدورمجوزهای بازاری برای تولید وتوزیع برخی محصولات خاص ومورد نیاز برای بخش آورژانس سلامت عمومی بودهاست. تولیدکننگان خودرو و سایرتولیدکنندگان محصولات غیرپزشکی نیزممکن است برای کمک به افزایش تجهیزات وملزومات تجهیزاتی مانند دستگاه اکسیژنرسان وارد عمل شوند، اما ابتدا باید درکی بهترازآییننامهها واستانداردهای مخصوص تجهیزات پزشکی بهدستآورند.
درادامه، ما بررسی خواهیم که چطور تولیدکنندگان ممکن است نسبت به درخواست صدرومجوزلازم به سازمان غذا و دارو برای مجازدانستن استفاده ازیک سری تجهیزات خاص وبه کارگیری عوامل قانونی که تولیدکنندگان محصولات غیرپزشکی باید ازآنها حین لحاظ کردن ابزارورزی ونوسامان سازی تجهیزات وامکانات خود جهت کمک به رسیدگی وبرطرفسازی نیاز به دستگاههای اکسیژنرسان ودیگرتجهیزات مراقبت پزشکی آگاه باشند، اقدام کنند.
معیارهای صدورمجوزاستفاده اورژانسی به سازمان غذا ودارو به همراه ارائه درخواست
ابتدا سازمان غذا ودارومجوزاستفاده اورژانسی ازتجهیزات پزشکی ازجمله کیتهای تست به کمک “تجهیز تشخیصی آزمایشگاهی” ( IVD- In Vitro Diagnostic ) برای تشخیص کووید 19 به همراه تجهیزات حفاظت شخصی (PPE) مانند رسپیراتور(افزاری برای دادن تنفس مصنوعی یا یاری رساندن به تهویه ریوی) نصب شونده روی صورت وفیلترکننده مورد نیازبرای حفاظت از کادردرمانی حین مراقبت ازبیماران.را صادرکرده است. به علاوه، سازمان غذا ودارو یک راهنمایی نهایی را درزمینه تجهیزات اکسیژنرسان که تسهیلبخش اجرای قواعد مجوزاستفاده اورژانسی برای این محصولات جهت درمان بیماران مبتلا به کووید 19 هستند، منتشرکردهاست.
براساس بیانیههای نهاد صدورمجوزاستفاده اورژانسی، سازمان غذا ودارو دارای اختیارصدورمجوزاستفاده اورژانسی وسریع وسائل خاص ازطریق بررسی وآزمایش پیشبازاری تسریعیافته حین بروزبحرانهای سلامت عمومی مانند شیوع بیماری همهگیرکووید 19 است.
معیارهای کلیدی برای حصول مجوزاستفاده اورژانسی ازسازمان غذا وداروبه شرح زیرهستند:
- حضوریک عامل شیمیایی، بیولوژیکی، رادیولوژیکی یا هستهای (دراین مورد، کروناویروس) که باعث تحمیل یک وضعیت یا بیماری جدی وخطرناک میشود؛
- صدورمجوزبرای استفاده ازیک وسیله خاص باید تامینکننده استاندارد ازنوع “ممکن است موثرباشد” برای درمان وضعیت یا بیماری هدف (دراین حالت، کووید19) باشد که موجب یک سطح آستانه کمترازمستندات موردنیازدرمقایسه با معیار”اثربخشی” استاندارد سازمان غذا ودارو به کارگرفتهشده درتحقیقات پیشبازاری نرمال میشود.
- توانایی سازمان غذا وداروبرای تعیین مزایای بالقوه وشناختهشده وسیله ازطریق تحلیل مزیت-ریسک درزمینه درمان، تشخیص یا پیشگیری ازبیماری کووید 19.
- عدم وجود درمانهای جایگزین موجود یا تاییدشده وکافی توسط سازمان غذا ودارو.
درخواست برای صدورمجوز استفاده اورژانسی
تولیدکنندگانی که درپی دریافت مجوزاستفاده اورژانسی ازیک سری تجهیزات خاص ومدنظرهستند ابتدا باید فعالیتهای مقدماتی قبل ازصدورمجوزرا آغازکنند وبا سازمان عذا وداروجلسه برگزارکنند تا شرایط بالقوه را به بحث بگذارند. انجام این مرحله، مخصوصا، برای شرکتهایی توصیه میشود که تجهیزات آنها درمراحل پیشرفته وپایانی توسعه قراردارد چرا که دستیابی سریع به کادردرمانی موضوعی حیاتی است.
سپس، یک تولیدکننده باید یک درخواست صدورمجوزاستفاده اورژانسی و رسمی را تسلیم سازمان غذا ودارو کند. این درخواست باید دربرگیرنده دادههای لازم وکافی درزمینه مسائل ایمنی؛ اثربخشی ومرتبط به ریسک درباره تجهیزات مدنظرباشد. عمق وپهنای چنین اطلاعاتی تا حد زیادی وابسته به این موضوع است که ایا یک وسیله معرفیشده برای یافتن مجوزاستفاده اورژانسی جهت استفاده به تازگی توسط سازمان غذا و داروتایید شدهاست یا خیر و یا اینکه ایا یک قاعده درمورد صدورمجوزاستفاده اورژانسی ازیک وسیله خاص موجب استفاده ازیک وسیله ازپیش تایید شده بهشکلی که برای آن منظورطراحینشده باشد، خواهد شد یاخیر.
برنامه زمانی برای تصمیمگیری درمورد وبررسی درخواست صدورمجوزاستفاده اورژانسی طبق بیانیه سازمان غذا ودارو بریک پایه مورد به مورد ایجاد میشود، اما آژانس معمولا این برنامهها را طی چند ساعت یا طی چند روزهم منتشرخواهد کرد اگرتولیدکنندگان معیارهای لازم را محقق کردهباشند وفعالیتهای لازم قبل ازصدرومجوزرا انجام دادهباشند.
صدورمجوزبرای چه مدت اعتباردارد؟
هرچند دریافت مجوزاستفاده اورژانسی ازتجهیزات مدنظرفراهمآورنده دستیابی سریع به بازارمراقبت بهداشتی آمریکا است، اما چنین مجوزهایی تازمانی اعتبارخواهند داشت که وضعیت اورژانسی درزمینه سلامت عمومی ازمنظرسازمان غذا ودارو همچنان ادامه داشته باشد. آژانس تعیینکننده تاریخهای موثربرای استفاده ازمجوزاستفاده اورژانسی است ودرپایان یک دوره اعلامیه صدورمجوزاین اختیارات خاص منقضی میشوند. تولیدکنندگان تجهیزات تایید وتعیینشده توسط سازمان صدورمجوزاستفاده اورژانسی که قبلا مجوزبازاری سازمان غذا ودارو را دریافت نکردهاند باید تجهیزات تولیدی خود را ازبازارمربوطه درآمریکا جمعاوری کنند؛ برای تجهیزات تاییدشده برای دیگراستفادههای مدنظرخارج ازبرد مجوزاستفاده اورژانسی، تولیدکنندگان باید اطمینان حاصل کنند که چنین تجهیزاتی به “استفاده معمول” بازمیگردند (ازچنین تجهیزاتی استفاده معمول خواهد شد).
ملاحظات مرتبط به تولیدکنندگان محصولات غیرپزشکی
سازمان غذا ودارودرجدیدترین راهنمایی خود درزمینه نظارت بردستگاههای اکسیژنرسان ودیگرتجهیزات تنفسی که عرضه آنها درآمریکا به میزان کافی نیست به دنبال توسعه موجودبودن این دستگاهها تاحدی به واسطه فراهمسازی صدورمجوز برای شرکتهای واجد شرایط ازجمله شرکتهای بدون تجربه قبلی درزمینه تولید تجهیزات پزشکلی اما علاقهمند به انجام این کار جهت کمک به رفع کمبودها است.
جالب اینکه، سازمان غذا ودارو قوبا تولیدکنندگان محصولات غیرپزشکی دارای پتانسیل افزایش محصولات اکسیژنرسان وسایرمحصولات مشابه را ترغیب میکند که مجوزلازم برای استفاده اورژانسی حین شیوع بیماری کووید 19 بگیرند. شرکتهای علاقهمند باید رویکردهای پیشنهادی خود را برای رفع مشکل تولید وعرضه به سازمان غذا وداروایمیل کنند.
راهنمایی نهایی همچنین به تولیدکنندگان برای اصلاح مولفهها یاکارکردهای تجهیزات اکسیژنرسان بدون ارئه گزارشهای پیشبازاری درزمینه تامین استاندارد همارز 510 (k) به آزانس برای دوره شیوع کووید 19 انعظافپذیری بیشتری را میدهد. چنین رویکردی برای کمک به تولیدکنندگانی لحاظ شدهاست که میخواهند تعداد خطوط محصول یا تولید را درمحلهای جایگزین که ممکن است طبق نظرآزانس تجهیزات تولیدی مختلفی برای افزایش ظرفیت تولید وعرضه به همراه کاهش موانع تولید وعرضه داشته باشند، افزایش دهند.
این رویکرد دررا برای همکاری بیشتربین آزانس وتولیدکنندگان صنعتی/خودرو با ظرفیت توسعه تولید تجهیزات مورد نیاز اما با تجربه کمتردرزمینه پرداختن به ورعایت استانداردها وآییننامههای مخصوص وسیله بازمیکند.
آییننامهها واستاندارهای بهشکلی بالقوه کاربردی سازمان غذا و دارو
تولیدکنندگان محصولات غیرپزشکی باید از استانداردهای کیفیت، امنیت وعملکردی که سازمان غذا و دارو معمولا خواهان رعایت آنها درزمینه تولید واصلاح مواد، سختافزارونرمافزاردستگاه اکسیژنرسان است آگاه باشند؛ تولیدکنندگان بخش صنعت و خودروممکن است نیازداشته باشند که رویکردها وفرایندهای موجود را تنظیم کنند تا این ملزومات محقق شوند. استانداردهای مرتبط دراین زمینه دربرگیرنده موارد زیراست:
- استانداردهای گروه60601 IEC برای تجهیزات الکتریکی- پزشکی
- IEC 62304 برای فرایندهای چرخهعمر نرمافزارتجهیزپزشکی
- ISO 10993 برای ارزیابی بیولوژیکی تجهیزات پزشکی
- استانداردهای گروه ISO 80601 برای تجهیزات الکتریکی-پزشکی ازجمله تجهیزات کمک تنفسی واکسیژنرسان.
شرکتها باید به سند راهنمایی ونهایی سازمان غذا ودارو برای مشاهده لیست کامل آییننامهها واستانداردهای کاربردی مراجعه کنند. برخی ازاین ملزومات ممکن نیست کاملا حین دوره اعتبارمجوزاستفاده اورژانسی ازوسیله اعمال شوند، اما تولیدکنندگان علاقهمند به حفظ محصولات خود دربازارآمریکا برای مدتزمانی طولانیتردرنهایت باید پیروی کامل خود را نشان دهند.
شروط احتمالی سازمان غذا ودارو برای اعطا مجوزاستفاده اورژانسی ازتجهیزات پزشکی به تولیدکنندگان محصولات غیرپزشکی
هرچند نهاد صدورمجوزاستفاده اورژانسی ازتجهیزپزشکی ازبرخی ملزومات تاییدی ارائه شده توسط سازمان غذا ودارو چشمپوشی میکند، آژانس شروطی را مطرح میکند که احتمالا باید به منظورحصول مجوزبرای تولید وعرضه تجهیزات کمک تنفسی واکسیژنرسان به میزان زیاد موردنیازتامین شوند:
- آگاهی بخشی به متخصصین مراقبتبهداشتی و بیمارانن مبنی براین که سازمان غذا ودارواین تجهیزات را برای استفاده اورژانسی مجازدانسته وهمچنین ارائه دادههای سود-ریسک مرتبط وموجود
- ایجاد فرایندهایی برای ارزیابی وگزارش رخدادهای بحرانی ومرتبط به استفاده اورژانسی ازاین تجهیزات
- ثبت وگزارش مستمرفرایند استفاده اورژانسی ازاین وسائل
[/et_pb_text][/et_pb_column][/et_pb_row][/et_pb_section]